rituximab เป็นยาจากกลุ่ม cytostatics เป็นโมโนโคลนอลแอนติบอดีที่ส่วนใหญ่ใช้ในการรักษามะเร็งต่อมน้ำเหลืองที่เป็นมะเร็ง
rituximab คืออะไร?
Rituximab ได้รับการพัฒนาโดย Lee Nadler ที่ Dana-Farber Cancer Institute ในปี 1990 เป็นแอนติบอดีตัวแรกที่ได้รับการรับรองจากทั่วโลกในการรักษามะเร็ง ในสหภาพยุโรป Roche จำหน่าย Rituximab ภายใต้ชื่อทางการค้าMabThera®
ยาที่ผลิตด้วยเทคโนโลยีชีวภาพส่วนใหญ่จะใช้ในสหภาพยุโรปสำหรับการบำบัดด้วยภูมิคุ้มกันโรคมะเร็ง แต่ยังได้รับการอนุมัติสำหรับการรักษาโรคแพ้ภูมิตัวเอง ผลข้างเคียงค่อนข้างบ่อยเมื่อทาน rituximab ผู้ป่วยมะเร็งมากกว่าครึ่งมีไข้ผื่นหรือหายใจลำบาก ผู้ป่วยโรคข้ออักเสบรูมาตอยด์ทนต่อสารนี้ได้ดีกว่า ผลข้างเคียงที่ร้ายแรงเช่น Stevens-Johnson syndrome หรือ necrolysis epidermal necrolysis นั้นหายาก
ฤทธิ์ทางเภสัชวิทยา
Rituximab เป็นโมโนโคลนอลแอนติบอดี อิมมูโนโกลบูลิน IgG kappa ถูกนำไปต่อต้านแอนติเจนที่พื้นผิว CD20 แอนติเจนพื้นผิวนี้ส่วนใหญ่พบบนพื้นผิวของ B lymphocytes CD20 พบได้ในเนื้องอก B-cell เกือบทั้งหมด การใช้ rituximab ในมะเร็งจะมีประโยชน์ก็ต่อเมื่อเซลล์มะเร็งมีโมเลกุลที่พื้นผิว CD20 ในเซลล์เหล่านี้ rituximab จะผูกกับ CD20 สิ่งนี้สร้างความซับซ้อนที่กระตุ้นการตอบสนองภูมิคุ้มกันของร่างกาย
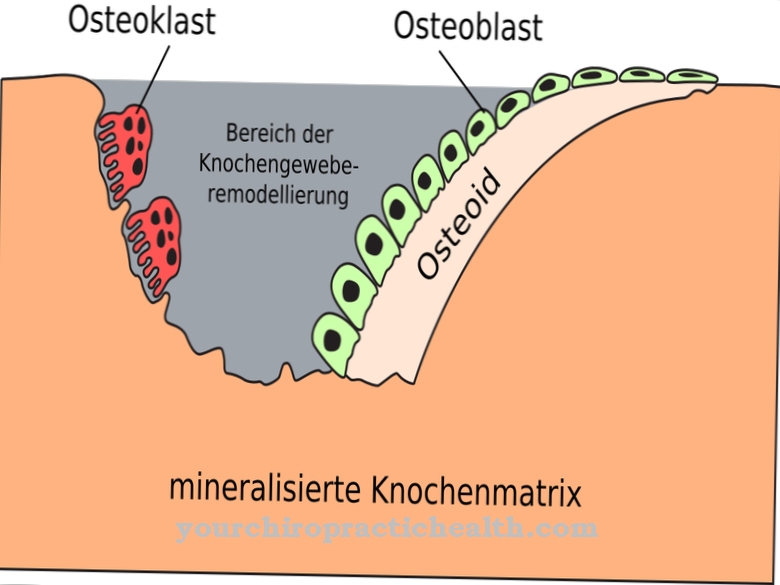
การทำลายเซลล์ที่แสดงออกนั้นเริ่มต้นโดยกลไกการทำงานที่แตกต่างกันสามแบบ ในอีกด้านหนึ่งการตายของเซลล์ที่ตั้งโปรแกรมไว้ (apoptosis) จะเริ่มขึ้นในเซลล์ที่ได้รับผลกระทบ ในกระบวนการนี้เซลล์จะแยกตัวออกจากเนื้อเยื่อก่อน พวกมันมีสีอีโอซิโนฟิลิกมากขึ้นและมีขนาดเล็กลง แผลพุพองบนเยื่อหุ้มเซลล์ นิวเคลียสของเซลล์ก็หนาแน่นขึ้นเรื่อย ๆ และมีขนาดเล็กลง ในตอนท้ายของการตายของเซลล์ร่างกายยังคงมีการตายของเซลล์ขนาดเล็กซึ่งจะถูกกำจัดโดย phagocytosis ด้วยการตายของเซลล์ตามโปรแกรมจะไม่มีปฏิกิริยาการอักเสบ
นอกเหนือจากการตายของเซลล์แล้วการสลายตัวของเซลล์ B ที่ขึ้นกับส่วนประกอบยังพัฒนาอีกด้วย ปัจจัยต่าง ๆ ของส่วนประกอบที่ตอบสนอง ระบบเสริมเป็นระบบที่มีลักษณะคล้ายน้ำตกในพลาสมาโปรตีน ในตอนท้ายของน้ำตกสิ่งเหล่านี้จะกระตุ้นการตอบสนองของแอนติบอดีซึ่งเซลล์ที่ได้รับผลกระทบถูกโจมตี ตามมาด้วยปฏิกิริยาการอักเสบและการทำลายเซลล์ในที่สุด
กลไกการออกฤทธิ์ที่สามขึ้นอยู่กับความเป็นพิษต่อเซลล์ของเซลล์ที่ขึ้นกับแอนติบอดี Rituximab ดึงดูด macrophages, granulocytes และ T cells ตามธรรมชาติซึ่งจะกำจัดเซลล์ที่ได้รับผลกระทบ
การประยุกต์ใช้และการแพทย์
Rituximab ส่วนใหญ่ใช้ในการรักษามะเร็ง ยานี้เป็นส่วนหนึ่งของการบำบัดมาตรฐานสำหรับมะเร็งต่อมน้ำเหลืองชนิดที่ไม่ใช่มะเร็งต่อมน้ำเหลืองและฟอลลิคูลาร์ที่ไม่ใช่ Hodgkin มะเร็งต่อมน้ำเหลืองชนิด Non-Hodgkin เป็นโรคร้ายของระบบน้ำเหลืองที่ไม่ใช่โรค Hodgkin ต่อมน้ำเหลืองแสดงว่าต่อมน้ำเหลืองขยายตัวโดยไม่เจ็บปวดเหนื่อยน้ำหนักลดมีไข้เหงื่อออกตอนกลางคืนหรือมีความไวต่อการติดเชื้อเพิ่มขึ้น
ในกรณีเหล่านี้มักใช้ rituximab ร่วมกับเคมีบำบัดแบบเดิม มักใช้โครงการ CHOP ซึ่งรวมถึงยา cyclophosphamide, daunorubicin, vincristine และ prednisolone การศึกษาแสดงให้เห็นว่าการใช้โปรโตคอล CHOP ร่วมกับ rituximab มีผลดีต่อการพยากรณ์โรค
Rituximab เป็นหนึ่งในยาที่สำคัญที่สุดที่ใช้ในการรักษามะเร็งต่อมน้ำเหลืองที่เกี่ยวข้องกับการปลูกถ่าย เหล่านี้เป็นโรคมะเร็งที่คล้ายมะเร็งต่อมน้ำเหลืองที่เกิดขึ้นหลังจากการปลูกถ่ายอวัยวะหรือเซลล์ต้นกำเนิด
Rituximab ยังใช้ร่วมกับยา Bendamustine เพื่อรักษามะเร็งเม็ดเลือดขาวเม็ดเลือดขาวชนิดเรื้อรังขั้นสูง อย่างไรก็ตามการศึกษาล่าสุดระบุว่าผลการรักษาดีขึ้นเมื่อใช้ rituximab ร่วมกับ cyclophosphamide และ fludarabine
เมื่อยามาตรฐานและตัวยับยั้ง TNF-αเริ่มต้นล้มเหลว rituximab ยังใช้ในการรักษาโรคข้ออักเสบรูมาตอยด์ โรคข้ออักเสบรูมาตอยด์เป็นการอักเสบเรื้อรังของข้อต่อซึ่งก่อนหน้านี้รู้จักกันในชื่อโรคไขข้ออักเสบ โดยปกติข้อต่อนิ้วจะได้รับผลกระทบ สำหรับผู้ป่วยจำนวนมากการให้ยาสองครั้งภายในสองสัปดาห์สามารถช่วยให้อาการดีขึ้นในช่วงเวลาหนึ่งปี แนะนำให้ใช้ช่วงการรักษาหกเดือน การให้ยาเพิ่มเติมสามารถรักษาหรือปรับปรุงความสำเร็จของการรักษาได้
ข้อบ่งชี้อีกประการหนึ่งสำหรับการใช้ rituximab คือ glomerulonephritis โรคอักเสบเรื้อรังของเนื้อไตเกิดจากการสร้างแอนติบอดีต่อโปรตีนของเซลล์ไต
คุณสามารถหายาของคุณได้ที่นี่
➔ยาเพื่อเสริมสร้างการป้องกันและระบบภูมิคุ้มกันความเสี่ยงและผลข้างเคียง
ในด้านเนื้องอกวิทยาผู้ป่วยมากกว่า 50 เปอร์เซ็นต์เกิดผลเสีย ซึ่งรวมถึงไข้หายใจลำบากผื่นและหนาวสั่น อาการรุนแรงน่าจะเกิดจากการสลายตัวของเซลล์มะเร็งที่ถูกทำลายไปมาก ไซโตไคน์จำนวนมากถูกปล่อยออกมาในระหว่างการสลายนี้ Cytokines เป็นโปรตีนที่มีบทบาทสำคัญในปฏิกิริยาภูมิคุ้มกันและกระบวนการอักเสบอาการที่เกิดขึ้นในระหว่างการสลายตัวจึงสรุปได้เช่นกันภายใต้คำว่า cytokine release syndrome กลุ่มอาการนี้ส่วนใหญ่เกิดขึ้นในผู้ป่วยที่มีก้อนเนื้องอกขนาดใหญ่ ผลข้างเคียงเหล่านี้มักจะดีขึ้นเมื่อได้รับการรักษา
ผู้ป่วยมะเร็งแต่ละรายอาจมีการพัฒนา leukoencephalopathy multifocal แบบก้าวหน้า (PML) ในระหว่างการรักษา สมองถูกโจมตีโดยไวรัส JC เนื่องจากภูมิคุ้มกันบกพร่อง การติดเชื้อไวรัสฉวยโอกาสเป็นอันตรายถึงชีวิตได้เสมอ กรณี PML ส่วนใหญ่เกิดขึ้นในผู้ป่วยมะเร็งต่อมน้ำเหลืองและในระหว่างการรักษาร่วมกับยาพิษต่อเซลล์ภูมิคุ้มกัน กรณี PML เป็นที่รู้จักในผู้ป่วยที่เป็นโรคแพ้ภูมิตัวเอง
ผลข้างเคียงที่ร้ายแรงเช่น Stevens-Johnson syndrome และ necrolysis epidermal necrolysis เกิดขึ้นในผู้ป่วยที่ได้รับการรักษาน้อยกว่า 0.01 เปอร์เซ็นต์

.jpg)







.jpg)